Gyvsidabrio junginių reakcijos
Metalinis gyvsidabris ir jo junginiai yra labai toksiški gyviems organizmams. Tai ypač pasakytina apie junginius, kurie gerai tirpsta vandenyje. Eksperimentuojant su šio unikalaus elemento deriniais reikia būti labai atsargiems (gyvsidabris yra vienintelis metalas, kuris kambario temperatūroje yra skystas). Pagrindinių chemiko nurodymų laikymasis? leis jums saugiai atlikti keletą eksperimentų su gyvsidabrio junginiais.
Pirmuoju eksperimentu gauname aliuminio amalgamą (šio metalo tirpalą skystame gyvsidabryje). Gyvsidabrio (II) tirpalas Hg nitratas (V) Hg (NO3)2 ir aliuminio vielos gabalas (1 nuotrauka). Aliuminio strypas (atsargiai išvalytas nuo nuosėdų) dedamas į mėgintuvėlį su tirpios gyvsidabrio druskos tirpalu (2 nuotrauka). Po kurio laiko galime stebėti dujų burbuliukų išsiskyrimą nuo laido paviršiaus (3 ir 4 nuotraukos). Išėmus strypą iš tirpalo, paaiškėja, kad molis pasidengęs puria danga, o be to dar matome metalinio gyvsidabrio kamuoliukus (5 ir 6 nuotraukos).
Chemija – gyvsidabrio jungimo patirtis
Įprastomis sąlygomis aliuminio paviršius yra padengtas sandariai priglundančiu aliuminio oksido sluoksniu.2O3efektyviai izoliuoja metalą nuo agresyvaus aplinkos poveikio. Išvalius ir panardinus strypą į gyvsidabrio druskos tirpalą, Hg jonai išstumiami2+ aktyvesnis aliuminis
Ant strypo paviršiaus nusėdęs gyvsidabris sudaro amalgamą su aliuminiu, todėl oksidui sunku prilipti prie jo. Aliuminis yra labai aktyvus metalas (reaguodamas su vandeniu išskiria vandenilį – stebimi dujų burbuliukai), o jo kaip konstrukcinės medžiagos panaudojimas galimas dėl tankios oksidinės dangos.
Antrajame eksperimente aptiksime amonio NH jonus.4+ naudojant Neslerio reagentą (1856 m. pirmasis jį analizei panaudojo vokiečių chemikas Julius Nesleris).
Apynių ir gyvsidabrio junginių reakcijos eksperimentas
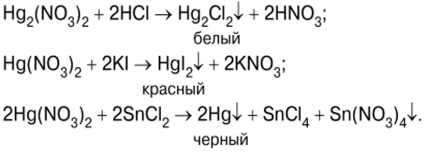
Bandymas prasideda gyvsidabrio(II) jodido HgI nusodinimu.2, sumaišius kalio jodido KI ir gyvsidabrio (II) nitrato (V) Hg (NO) tirpalus3)2 (7 nuotrauka):
Oranžinės raudonos HgI nuosėdos2 (8 nuotrauka), tada apdorotas kalio jodido tirpalo pertekliumi, kad gautų tirpų kompleksinį junginį, kurio formulė K2HgI4 ? Kalio tetrajoderkuratas (II) (9 nuotrauka), kuris yra Nesslerio reagentas:
Su gautu junginiu galime aptikti amonio jonus. Vis tiek reikės natrio hidroksido NaOH ir amonio chlorido NH tirpalų.4Cl (10 nuotrauka). Į Neslerio reagentą įpylus nedidelį kiekį amonio druskos tirpalo ir terpę šarminant stipria baze, stebime mėgintuvėlio turinio geltonai oranžinės spalvos susiformavimą. Dabartinę reakciją galima parašyti taip:
Gautas gyvsidabrio junginys turi sudėtingą struktūrą:
Itin jautrus Nessler testas naudojamas net amonio druskų ar amoniako pėdsakams aptikti vandenyje (pvz., vandentiekio vandenyje).

